Z5 - Molekulare Mechanismen der Wirkung von Adipokinen
Adipokine werden aus dem Fettgewebe freigesetzt und beeinflussen den Stoffwechsel des gesamten Organismus. Dementsprechend führt erhöhtes Körperfett zu einer erhöhten oder reduzierten Freisetzung von Adipokinen – abhängig von ihrer Regulierung. Dies kann im weiteren die Disfunktion bei Adipositas erklären. Verschiedene Adipokine wurden mit Adipositas in Verbindung gebracht, darunter Adiponektin, Vaspin, Dlk1/Pref-1 (delta-like homolog 1; preadipocyte factor 1) und Chemerin. Bisher ist aber nur wenig über den molekularen Mechanismus der Funktion bekannt. Wir konnten erfolgreich in ganzer Länge und globular Adiponektin, Vaspin, Dlk1/Pref-1 und Chemerin klonieren und exprimieren. Diese Adipokine wurden durch genetische Studien oder Expressionsanalysen in viszeralem oder subkutanem Fett identifiziert. Ziel des Projektes ist es nun, die Ziele der Adipokine zu identifizieren, neue Interaktionspartner zu finden und die molekularen Mechanismen ihrer physiologischen Aktivitäten zu erhellen. Wir stellen die Hypothese auf, dass die Site-spezifischen und selektiv markierten Adipokine neue Zielmoleküle für die Interaktion ergeben werden und es erlauben, die Adipokin-Funktion und ihre Rollen bei Adipositas erhellen werden. Im 1. Abschnitt des Projektes werden wir Adiponektin, Vaspin, Dlk1/Pref-1 und Chemerin untersuchen, deren wichtige Rolle bei Adipositas und damit verbundenen Stoffwechselerkrankungen bereits gezeigt wurde. Die Proteine werden für die Strukturanalyse rekombinant exprimiert und chemisch modifiziert, um Lokalisierungsstudien durchzuführen und Interaktionspartner durch Ko-Immunoprezipitation zu identifizieren. Einerseits werden Adipokine fluoreszenz-markiert, um ihre Verteilung und ihre Bindung an Zellen zu verfolgen sowie in vitro-Assays durchzuführen. Andererseits erlaubt die Biotin-Markierung die Ko-Immunoprezipitation von Adipokinen aus Zellultur, Überstand oder Blut und die Modifikation mit Chelatoren die Produktion von Gadolinium-markierten Adipokinen für MRT-Verteilungsstudien in lebenden Mäusen. Die so gewonnenen Informationen werden die Frage nach der Rolle dieser wichtigen Adipokine und ihrem Wechselspiel mit Adipositas beantworten.
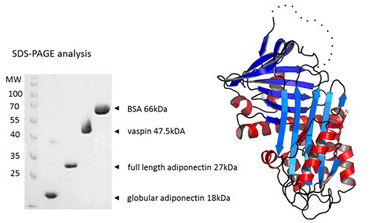
Abbildung 1: Expression und Charakterisierung von Vaspin, Adiponektin in voller Länge und globular, sowie der Kristallstruktur von Vaspin (wie publiziert in Heiker et al., Cell Mol Life Sci 2013.)
Fischer TF, Schoeder CT, Zellmann T, Stichel J, Meiler J, Beck-Sickinger AG. Cyclic Analogues of the Chemerin C-Terminus Mimic a Loop Conformation Essential for Activating the Chemokine-like Receptor 1. J Med Chem. 2021 Mar 25;64(6):3048-3058.
Ziffert I, Kaiser A, Hoppenz P, Mörl K, Beck-Sickinger AG. Shuttling of Peptide-Drug Conjugates by G Protein-coupled Receptors is Significantly Improved by Pulsed Application. ChemMedChem. 2020 Jul 22.
Jendrny C, Beck-Sickinger AG. Inhibition of kallikrein-related peptidases 7 and 5 by grafting serpin reactive-center loop sequences onto sunflower trypsin inhibitor-1 (SFTI-1). Chembiochem. 2016;17:719-26.
Saalbach A, Tremel J, Herbert D, Schwede K, Wandel E, Schirmer C, Anderegg U, Beck-Sickinger AG, Heiker JT, Schultz S, Magin T, Simon JC. Anti-inflammatory action of keratinocyte-derived vaspin: relevance for the pathogenesis of psoriasis. Am J Pathol. 2016;186:639-51.
Mattern A, Zellmann T, Beck-Sickinger AG. Processing, signaling and physiological function of chemerin. IUBMB Life. 2014;66:19-26.
Heiker JT, Klöting N, Kovacs P, Kuettner EB, Sträter N, Schultz S, Kern M, Stumvoll M, Blüher M, Beck-Sickinger AG. Vaspin inhibits kallikrein 7 by serpin mechanism. Cell Mol Life Sci. 2013;91:97-105.
Schultz S, Beck-Sickinger AG. Chemerin and Vaspin: Possible Targets to Treat Obesity? ChemMedChem. 2013;8:549-59.
Juhl C, Beck-Sickinger AG. Molecular tools to characterize adiponectin activity. Vitam Horm. 2012;90:31-56.
Saalbach A, Vester K, Rall K, Tremel J, Anderegg U, Beck-Sickinger AG, Blüher M, Simon JC. Vaspin-a link of obesity and psoriasis? Exp Dermatol. 2012;21:309-12.
Klöting N, Kovacs P, Kern M, Heiker JT, Fasshauer M, Schön MR, Stumvoll M, Beck-Sickinger AG, Blüher M. Central vaspin administration acutely reduces food intake and has sustained blood glucose-lowering effects. Diabetologia. 2011;54:1819-23.
Juhl C, Mörl K, Beck-Sickinger AG. Adiponectin receptor 1 interacts with both subunits of protein kinase CK2. Mol Cell Biochem. 2011;356:185-9.
Heiker JT, Kosel D, Beck-Sickinger AG. Molecular mechanisms of signal transduction via adiponectin and adiponectin receptors. Biol Chem. 2010;39:1005-18.
Kosel D, Heiker JT, Juhl C, Deckert CM, Blüher M, Mörl K, Beck-Sickinger AG. Adiponectin receptor 1 dimerisation is inhibited by adiponectin. J Cell Sci. 2010;123:1320-8.
Heiker JT, Klöting N, Blüher M, Beck-Sickinger AG. Access to gram scale amounts of functional globular adiponectin from E. coli inclusion bodies by alkaline-shock solubilization. Biophys Biochem Res Comm. 2010;398:32-7.
Heiker JT, Wottawah CM, Juhl C, Kosel D, Mörl K, Beck-Sickinger AG. Protein kinase CK2 interacts with adiponectin receptor 1 and participates in adiponectin signalling. Cell Signal. 2009;21:936-42.